食品に含まれる糖類とは?
食品表示法において糖類は「単糖類又は二糖類であって、糖アルコールでないもの」と定義されます。糖類には多くの種類がありますが、食品に含まれる主な糖類は、単糖類ではグルコース、フルクトース、ガラクトース、二糖類ではスクロース、ラクトース、マルトース、トレハロース、セロビオース、イソマルトースがあります。
弊社の糖類分析は、単糖類3種と二糖類の中のスクロース、ラクトース、マルトースの合計6糖類を一斉分析としています。
その他の二糖類であるトレハロースは、きのこ類に含まれており、さまざまな食品の食品添加物として使用されています。セロビオースはマツ葉やトウモロコシの茎に微量に含まれています。イソマルトースは、はちみつや味噌などの発酵食品に含まれています。これらの二糖類は、添加物として扱われること、含まれる食品が限られること、食品に含まれる量が微量であることから、弊社では一斉分析の項目としておりません。

<6糖類の構造>
図1に単糖類、図2に二糖類の構造を示します。単糖類は分子量が同じで似た構造をしており、二糖類は単糖類が2つ結合した構造をしています。そのため糖類は、似た特性・特徴をもつので分離が難しい物質です。官能基としては、水酸基(-OH)が多く存在するので極性が高く、水に容易に溶解する特徴があります。
◆単糖類
炭素原子が6個で構成された「ヘキソース(六炭糖)」の構造をしています。
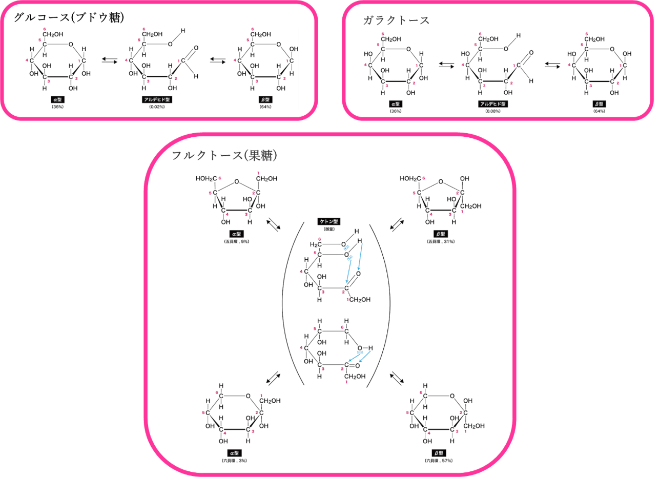
◆二糖類
2つの単糖類が下記のように結合してできています。
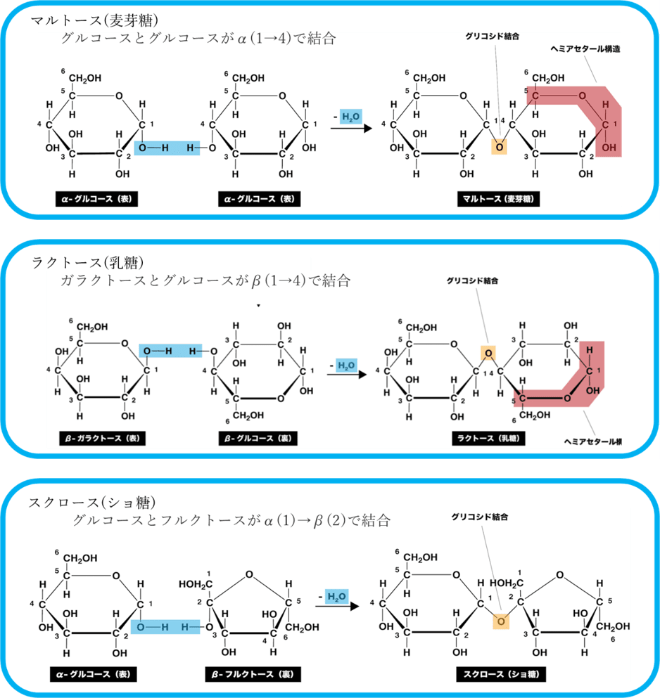
<糖類の分離方法>
食品中の糖類の分析は、主に高速液体クロマトグラフ(HPLC)を使用します。構造上分離が難しい糖類ですが、水への溶解性の高さや、水酸基の特性を活かした反応、pHによるイオン化を利用し、下記のような様々な方法で分離をしています。
①サイズ排除
分子量の大きさにより分離する方法で、多糖類と単糖・二糖類の分離に適していますが、同一分子量の分離は困難です。
②配位子交換
糖類のもつ水酸基とカラムがもつ金属対イオンが錯形成し、その安定性の差を利用して分離します。単糖・二糖類の分離に適しています。しかし、溶離液が純水のみのため、移動相組成やグラジエントによる分離は同時に行えません。
③順相:HILIC
極性の高い糖類は、極性の高いアミノプロピル基を官能基として持つカラムを使用し、移動相に水・アセトニトリル混液を用いて分離します。水の割合が高くなるほど早く溶出します。
④陰イオン交換
中性糖類のpKaは12程度(例. グルコース:12.28)であることから、糖類は弱酸性といえます。そのため、強塩基性移動相内では部分的にイオン化され、陰イオン交換樹脂に保持させることができます。一般に、移動相には水酸化ナトリウム水溶液が使用され、単糖類からオリゴ糖の順に溶出します。
<糖類分析に使用する検出器>
HPLC分析に使用する検出器は、必要に応じて選択することが可能です。以下、検出器について簡単に紹介します。
①紫外可視検出器(UV/VIS)
6糖類の構造で示した通り、糖類の主な官能基は水酸基(-OH基)です。そのため、紫外吸収がとても低いため、実分析には適していません。
②示差屈折検出器(RID)
糖類の分析で最も使用されている検出器です。弊社の分析では、この示差屈折検出器を使用して行っています。定量性があり、再現性も高く、操作が容易である利点があります。しかし、分析時の温度の影響を受けやすく、グラジエントをかけた分析ができないため、感度があまり高くないことや、移動相と異なる屈折率を持つ化合物をすべて検出するため、検出選択性が低いと言えます。
③蛍光検出器(FLD)
蛍光検出は、検出選択性や感度が優れていますが、糖類は発蛍光性ではないため、蛍光誘導体化を行う必要があり、操作性が他の検出器に比べ劣ります。誘導体化はプレカラム法とポストカラム法があります。
④電気化学検出器(ED)
化合物の酸化・還元反応で生じた電流を測定する検出器のため、反応液を強アルカリにする必要があり操作上不利な点がありますが、検出感度がとても高いです。
⑤蒸発光散乱検出器(ELSD)
カラム溶出液を噴霧して移動相を蒸発させ、化合物を微粒子化したものに光を当てて発生した散乱光を検出する方法です。グラジエントをかけた分析が可能なため、検出選択性が高く、糖類の多成分同時分析に有用です。
<弊社で実施している分析方法>
上記の通り、弊社で行っている示差屈折検出器を使用した糖類分析では、「検出選択性が低い=夾雑との分離が困難」という問題があります。
この問題を解消するため、弊社では糖類の分離法に工夫を凝らしています。その一例を示します。
図3に6種の糖類標準品を一斉分析したクロマトグラム及び、塩分が多く含まれる食品のクロマトグラムを示します。このクロマトグラムから、フルクトースとグルコースのピーク位置に大きな塩分のピークが重なり、正確な測定ができない状態となっていることが分かります。
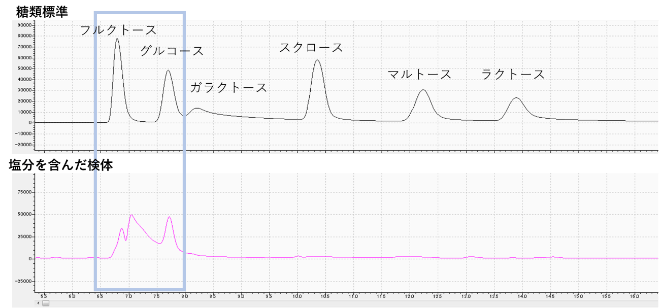
図4は図3で使用したカラムとは異なるカラムを用いて、同検体を分析したクロマトグラムです。塩の影響を受けることなく、グルコースとフルクトースのピークが確認できます。
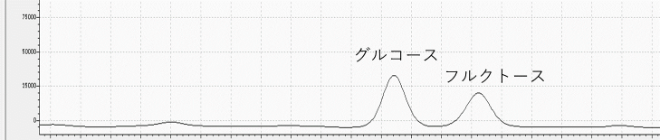
このように弊社では、検体の特徴を調査した上で、カラムの複数使用や、分離法の検討を行い、最適な分析法で計測を行っております。
糖類の検査方法について、ご質問・ご相談がございましたらご連絡ください。
糖類の検査はこちらから→
https://www.shokukanken.com/kensa_cat/foods/label/nutrition/
<引用元>
1. 栄養成分表示及び栄養強調表示とは
https://www.caa.go.jp/assets/food_labeling_cms206_20220531_02.pdf
2. 糖類の分離法、糖類の検出法 : 分析計測機器(分析装置) 島津製作所
https://www.an.shimadzu.co.jp/faq/example/lctalk-50intro/index.html
3. 化学のグルメ
https://kimika.net/t3tantou.html
4. 菓子類のしょ糖分の定量分析法
https://www.customs.go.jp/ccl_search/analysis_search/a_108_j.pdf
5. 公益財団法人 日本食品化学研究振興財団 既存添加物名簿
https://www.ffcr.or.jp/tenka/list/post-12.html?OpenDocument#list_20
